Rozhodnutí CHMP zahájit průběžný přezkum je založeno na předběžných výsledcích laboratorních studií (neklinické údaje) a časných klinických studií u dospělých. Tyto studie naznačují, že vakcína spouští dostatečnou produkci protilátek, které se zaměřují na SARS-CoV-2, virus způsobující onemocnění COVID-19, a může tak pomoci chránit před touto nemocí.
‼️ EMA starts #RollingReview of Valneva’s #COVID19vaccine.
— EU Medicines Agency (@EMA_News) December 2, 2021
Studies in adults show that this inactivated vaccine triggers the production of antibodies that target the #coronavirus.
👉 https://t.co/PSaOYnAyHp pic.twitter.com/RKqGkVzw9q
EMA bude průběžně hodnotit data, jakmile budou k dispozici, aby rozhodla, zda přínosy této vakcíny převažují nad jejími riziky. Průběžný přezkum bude pokračovat tak dlouho, dokud nebude k dispozici dostatek důkazů pro předložení formální žádosti o registraci.
EMA posoudí soulad dokumentace k VLA2001 s obvyklými standardy EU pro účinnost, bezpečnost a kvalitu. I když EMA nemůže předvídat délku posouzení, vyhodnocení případné žádosti by mělo trvat kratší dobu než obvykle právě kvůli průběžnému hodnocení. EMA bude informovat, jakmile bude předložena žádost o formální registraci.
O jaký typ vakcíny jde?
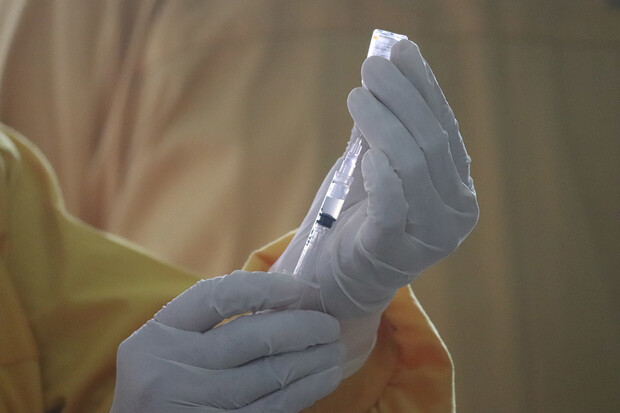
Vakcína VLA2001 obsahuje inaktivovaný (usmrcený) virus SARS-CoV-2, který však nemůže způsobit onemocnění COVID-19. VLA2001 také obsahuje látky (tzv. adjuvans), které pomáhají posílit imunitní odpověď na tuto vakcínu.
Když je člověku podána tato vakcína, jeho imunitní systém identifikuje inaktivovaný virus jako cizorodou částici a vytvoří proti němu protilátky. Pokud se později očkovaná osoba dostane do kontaktu se skutečným virem SARS-CoV-2, imunitní systém virus rozpozná a bude připraven se mu bránit.
Valneva and IDT Biologika Announce Collaboration for Production of Inactivated COVID-19 Vaccine VLA2001https://t.co/fD3OA6s69n pic.twitter.com/GqTEu0gQ8V
— Valneva (@valnevaSE) November 29, 2021