Výbor pro humánní léčivé přípravky (CHMP) EMA důkladně posoudil všechny potřebné údaje o kvalitě, bezpečnosti a účinnosti vakcíny a doporučil, aby Evropská komise vakcíně udělila podmínečnou registraci, která bude platná ve všech zemích EU/EHP.
Udělením této centralizované registrace mohou být občané EU ujištěni, že vakcína splňuje všechny evropské standardy, které se týkají zajištění kvality, bezpečnosti a účinnosti. Stejně jako u ostatních vakcín proti onemocnění COVID-19 bude i u této vakcíny po dobu její registrace nadále sledována její bezpečnost a účinnost. „Tato vakcína se liší od dříve registrovaných vakcín proti COVID-19, jde o takzvanou proteinovou podjednotkovou vakcínu, nejedná se tedy o očkovací látku založenou na mRNA nebo virovém vektoru. Věřím, že rozšíření spektra dostupných vakcín podpoří očkování, a tím dále zmírní dopad pandemie na naši společnost,“ říká ředitelka Státního ústavu pro kontrolu léčiv Irena Storová.
Výsledky ze dvou hlavních klinických studií prokázaly, že Nuvaxovid byl účinný v prevenci onemocnění COVID-19 u osob starších 18 let. Studie zahrnovaly celkem více než 45 000 účastníků. V první studii kolem 2/3 účastníků obdrželo vakcínu Nuvaxovid a zbylá 1/3 obdržela placebo (neúčinnou látku); v další studii obdržela polovina Nuvaxovid a polovina placebo. Účastnící studie nevěděli, zda obdrželi Nuvaxovid nebo placebo.
‼️ EMA recommends Nuvaxovid, the #COVID19vaccine developed by #Novavax, for authorisation in the 🇪🇺, to prevent #COVID19 in people from 18 years of age. #HealthUnion
— EU Medicines Agency (@EMA_News) December 20, 2021
👉 https://t.co/C0CrY8Jhih pic.twitter.com/bFDwTnh4Zf
První studie, která byla prováděna v USA a Mexiku, ukázala 90,4% snížení počtu příznakového onemocnění COVID-19 v době po uplynutí sedmi dnů po podání druhé dávky Nuvaxovid (14 případů COVID-19 z 17 312 očkovaných osob) ve srovnání s placebem (63 případů COVID-19 z 8 140 osob, které dostaly placebo). To znamená, že v této studii byla účinnost 90,4 %. Druhá studie prováděná ve Velké Británii také ukázala významný pokles příznakového onemocnění COVID-19 u osob očkovaných vakcínou Nuvaxovid (10 případů ze 7 020 osob) ve srovnání s osobami, které dostaly placebo (96 případů z 7 019 osob). To znamená, že v této studii byla účinnost 89,7 %.
Celkově tedy výsledky těchto dvou studií ukazují účinnost vakcíny Nuvaxovid kolem 90 %. Původní kmen SARS-CoV-2 a některé jeho varianty, jako je alpha a beta, byly nejběžnějšími virovými kmeny v době, kdy studie probíhaly. V současnosti jsou k dispozici omezené údaje o účinnosti vakcíny Nuvaxovid proti jiným variantám SARS-CoV-2, včetně varianty omikron. Studie sice nezahrnovaly účinnost proti variantě SARS-CoV-2 omikron, nicméně společnost Novavax již oznámila, že vyhodnocuje svou vakcínu proti této variantě, jak to společnost udělala pro předchozí varianty včetně alpha, beta a delta, a rovněž Novavax zahájil vývoj konstruktu vakcíny specifické pro omikron.
Podle souhrnných údajů o reaktogenitě, zahrnujících účastníky ve věku 18 let a starší zařazené do dvou studií fáze 3, kteří dostali alespoň jednu dávku vakcíny Nuvaxovid nebo placeba, byly nejčastějšími nežádoucími účinky citlivost v místě injekce (75 %), bolest v místě injekce (62 %), únava (53 %), myalgie (bolesti svalů) (51 %), bolest hlavy (50 %), malátnost (41 %), artralgie (bolesti kloubů) (24 %) a pocit na zvracení nebo zvracení (15 %). Nežádoucí účinky byly obvykle mírné až střední závažnosti.
Celkově byl výskyt nežádoucích účinků vyšší u mladších věkových skupin: výskyt citlivosti v místě injekce, bolesti v místě injekce, únavy, myalgie, bolest hlavy, malátnosti, artralgie a pocit na zvracení nebo zvracení byl vyšší u dospělých ve věku 18 až 65 let než u osob ve věku 65 let a starších. Bezpečnost a účinnost vakcíny bude dále sledována při používání ve všech členských státech Evropské unie pomocí farmakovigilančního systému EU a dalších studií prováděných farmaceutickou společností a evropskými autoritami.
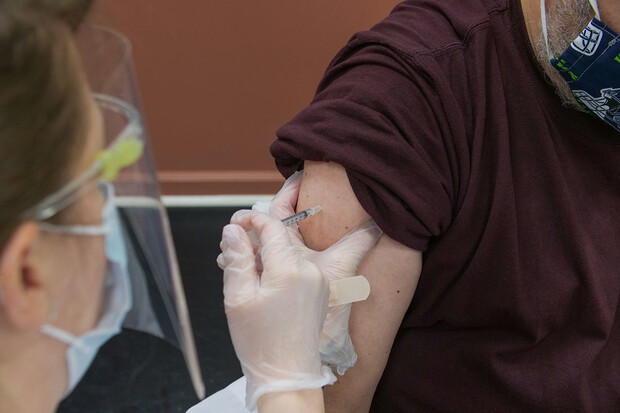
Vakcína Nuvaxovid se podává intramuskulárně (nitrosvalově), nejlépe do deltového svalu v horní části paže, ve dvou dávkách po 0,5 ml. Doporučuje se podat druhou dávku tři týdny po první dávce.
Jak vakcína Nuvaxovid funguje?
Stejně jako jiné vakcíny má Nuvaxovid připravit tělo na obranu proti virové infekci způsobené virem SARS-CoV-2. Vakcína obsahuje jako léčivou látku bílkovinu (protein) známou jako spike (S) protein, který je přítomen na povrchu koronaviru SARS-CoV-2. Když bude člověku podána tato vakcína, imunitní systém člověka pak bude s tímto proteinem zacházet jako s cizorodým a vytvoří proti němu přirozenou obranu – protilátky a T buňky (určitý typ buněk imunitního systému). Pokud později očkovaná osoba přijde do styku s virem SARS-CoV-2, imunitní systém tento virus rozpozná a bude připraven se proti němu bránit. Protilátky a imunitní buňky mohou společně zneškodnit virus, bránit jeho vstupu do buněk těla a ničit infikované buňky, což pomáhá chránit před onemocněním COVID-19. Vakcína Nuvaxovid rovněž obsahuje adjuvans, pomocnou látku, která posiluje reakci imunitního systému na vakcínu.